Notre intestin, appelé désormais « le deuxième cerveau », abrite près de 100 trillions de types de bactéries (1). On appelle cet « écosystème » le microbiote. Notre microbiote intestinal est important pour de nombreuses fonctions biologiques de l’organisme, notamment le développement intestinal, l’intégrité et la fonction de la barrière contre les pathogènes (2, 3), le métabolisme (4, 5), le système immunitaire (6) et le système nerveux central (SNC). Il existe des preuves solides d’échanges mutuels entre le stress et le microbiote (7). Cependant, les mécanismes de cette communication si particulière continuent d’être étudiés, il y a encore beaucoup d’aspects que nous ne connaissons pas sur le sujet. Dans cet article, nous verrons comment le microbiote influence le stress et quels sont les déterminants comportementaux.
Développement du cerveau humain
Le développement fonctionnel du cerveau des mammifères présente un intérêt particulier car les scientifiques ont découvert qu’il peut être sensible à des signaux environnementaux internes et externes pendant la vie périnatale. Des études épidémiologiques ont indiqué une association entre des troubles neurologiques, tels que l’autisme et la schizophrénie, et des infections par des agents pathogènes au niveau du microbiote pendant la période périnatale (8, 9).
De plus, l’exposition à des agents pathogènes microbiens pendant les périodes de développement entraîne des anomalies comportementales, notamment un comportement de type anxieux et une altération des fonctions cognitives (10-12).
On peut dire que toutes les bactéries ne sont pas forcément mauvaises. Mais pour notre microbiote, certaines sont bonnes (on les appelle aussi des probiotiques) et d’autres sont pathogènes. Une étude récente a montré que la bactérie, Bifidobacteria infantis, pouvait moduler positivement le métabolisme du tryptophane (un acide aminé responsable de l’hormone du bonheur), ce qui suggère que le microbiote intestinal normal peut influencer le réservoir de la sérotonine (13).
D’autre part, l’administration orale de certaines bactéries, comme la bactérie pathogène d’origine alimentaire, Campylobacter jejuni, entraîne un comportement de type anxieux chez les souris (14, 15).
Axe microbiote-intestin-cerveau
Microbiote et réponse au stress
Les scientifiques ont fait des recherches sur les rats axéniques.
Ces rats dépourvus de microbiote permettent d’observer comment l’existence – ou l’absence – d’un microbiote influence différents mécanismes. Les effets observés sont :
- une augmentation de la réactivité́ de l’axe corticotrope (le système central de réponse au stress),
- une influence de la réponse émotionnelle au stress,
- des modifications de réponse neuro-endocriniennes (les interactions entre le système nerveux et le système hormonal).
Photo de Robina Weermeijer sur Unsplash.com
Par quels mécanismes le microbiote intestinal agit-il sur la réponse au stress ?
On découvre peu à peu les voies de communication entre le microbiote et le cerveau, qui incluent le nerf vague, la signalisation hormonale intestinale, le système immunitaire, le métabolisme du tryptophane et les métabolites microbiens tels que les acides gras à chaîne courte.
Les acides gras à chaîne courte (AGCC) sont des acides gras comportant moins de six atomes de carbone. Issus de la fermentation microbienne intestinale d’aliments non-digestibles, les AGCC sont la principale source d’énergie du côlon, ce qui les rend essentiels à la santé gastro-intestinale. Ce sont tout simplement des sous-produits utiles, produits par les bonnes bactéries de ton colon.
Le nerf vague
Le nerf vague est composé à 90% de fibres ascendantes, qui transmettent des messages de l’intestin au cerveau. On sait aujourd’hui que le nerf vague transmet diverses informations, allant de la teneur en nutriments des aliments à la présence de produits bactériens (16). Les régions du cerveau qui reçoivent ces informations sont situées dans le tronc cérébral et l’hypothalamus et sont directement impliquées dans la réponse au stress (axe corticotrope).
Il est tout à fait possible qu’une modification de la composition du microbiote (qu’elle soit bénéfique ou néfaste) puisse avoir un impact sur notre humeur. L’ablation du nerf vague dans des modèles animaux supprime cet effet anxiolytique d’un microbiote sain, ce qui suggère que le nerf vague joue un rôle important dans la communication microbiote-cerveau (17-19).
La stimulation des cellules endocrines
Les nombreuses hormones libérées par le tractus intestinal, bien connues pour leurs effets métaboliques, ont également un impact sur le cerveau, les émotions et les comportements (20-22).
La composition du microbiote est déterminante pour notre métabolisme et peut affecter la production d’hormones par l’intestin. De plus, les hormones, enzymes et autres métabolites bactériens libérés par le microbiote lui-même ont également un effet sur le cerveau. C’est le cas des acides biliaires, des acides aminés et des acides gras à chaîne courte (23, 24).
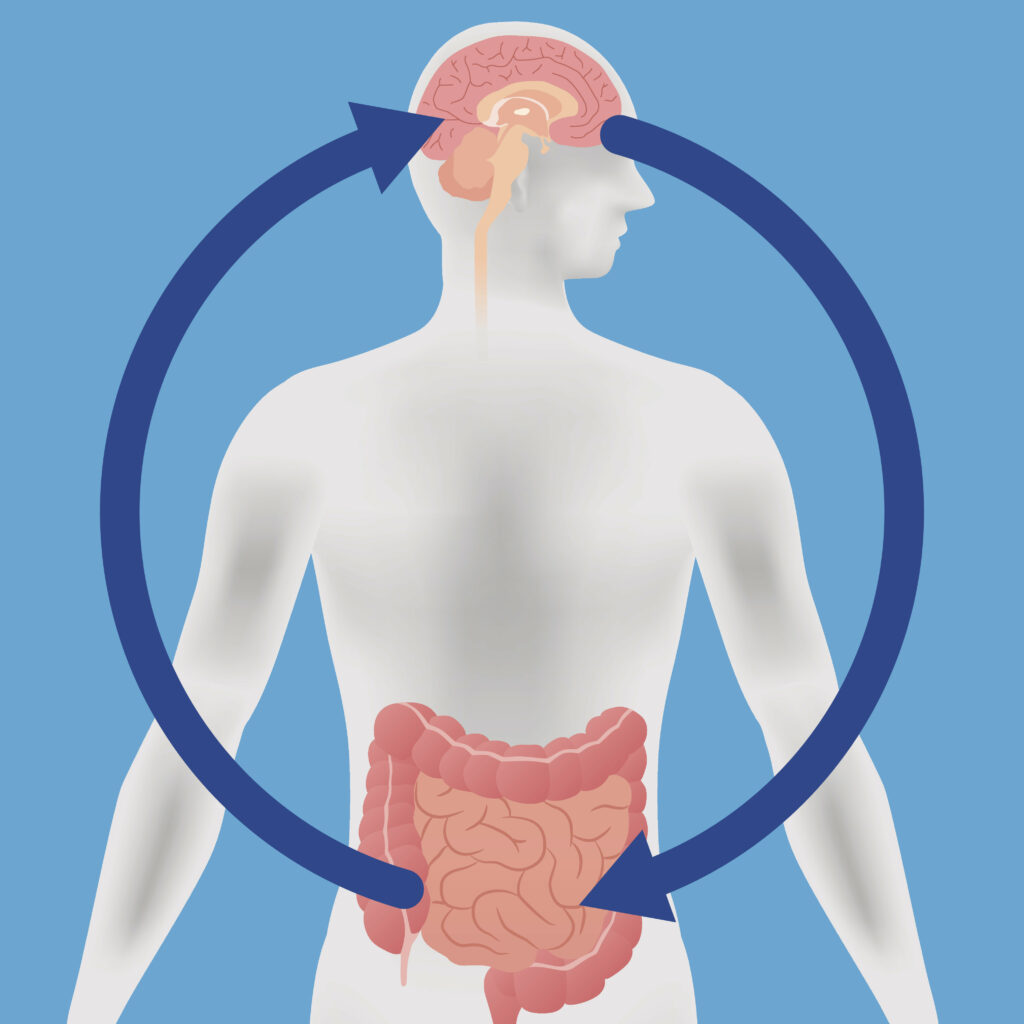
Photo de Harvard.edu
La production des cellules neuroactives
La modulation/création des transmetteurs (par exemple, la sérotonine, la mélatonine, l’acide gamma-aminobutyrique, les histamines et l’acétylcholine) dans l’intestin est un autre mécanisme d’action possible qui pourrait médier les effets du microbiote intestinal (25).
La sérotonine : C’est une substance chimique qui transmet des messages entre les cellules nerveuses du cerveau. La sérotonine joue un rôle clé dans des fonctions corporelles telles que l’humeur, le sommeil, la digestion, les nausées, la cicatrisation, la santé des os, la coagulation sanguine et le désir sexuel.
La mélatonine : Il s’agit d’une hormone que ton cerveau produit en réponse à l’obscurité. Elle contribue à la synchronisation de tes rythmes circadiens (horloge interne) et au sommeil.
L’acide gamma-aminobutyrique (GABA) : GABA est un neurotransmetteur, un messager chimique dans ton cerveau. Il ralentit le rythme de ton cerveau en bloquant des signaux spécifiques dans ton système nerveux central. Le GABA est connu pour produire un effet calmant.
Les histamines : Lorsque tu es stressé, ton corps libère des hormones et d’autres substances chimiques, dont l’histamine, la puissante substance chimique à l’origine des symptômes d’allergie.
L’acétylcholine : Il s’agit d’une substance chimique organique qui fonctionne dans le cerveau et le corps de nombreux animaux comme un neurotransmetteur. Des études cliniques ont suggéré qu’une augmentation de l’acétylcholine centrale pouvait entraîner un état dépressif.
La voie nerveuse
C’est la stimulation des neurones de notre système nerveux, qui influence le cerveau et la réponse au stress.
La voie immunitaire
Le microbiote effectue une stimulation des cellules immunitaires intestinales et modifie l’équilibre des cytokines inflammatoires (de petites protéines importantes dans la signalisation cellulaire). Ces cytokines peuvent augmenter l’inflammation, modifier le comportement et le stress en stimulant les systèmes nerveux périphérique et central (26, 27).
Le système nerveux comporte deux parties principales :
- Le système nerveux central est constitué du cerveau et de la colonne vertébrale.
- Le système nerveux périphérique est constitué de nerfs qui se branchent sur la colonne vertébrale et s’étendent à toutes les parties du corps.
On a constaté une importante régulation à la baisse des gènes liés au système immunitaire chez les souris sans microbiote (28), ce qui correspond à un système immunitaire et une microglie cérébrale qui seraient sous-développés (c’est un défaut de maturation du cerveau) (29). En effet, le système immunitaire peut constituer un lien essentiel pour les effets du microbiote sur la physiologie et le comportement du cerveau.
Peut-on modifier le microbiote pour gérer le stress ?
Nous sommes nombreux·ses à avoir déjà expérimenté les répercussions des émotions négatives et du stress sur la motilité intestinale. Les troubles digestifs tels que le syndrome du côlon irritable correspondent souvent à des troubles de l’humeur (33) et peuvent refléter une composition anormale du microbiote et une inflammation chronique associée (34). La manipulation du microbiote intestinal et de ses fonctions par les probiotiques et des comportements sains constitue une stratégie thérapeutique prometteuse.
Paradoxalement, bien que notre accès à la nourriture soit facilité, nous constations encore l’évolution croissante des maladies métaboliques liées à l’alimentation. Les habitudes alimentaires telles que les régimes riches en graisses et en sucre et pauvres en fibres ont augmenté les risques de maladies telles que le diabète, l’obésité ou les maladies inflammatoires de l’intestin. Tout cela touche également la santé de notre microbiote.

Photo de Anshu A sur Unsplash.com
Que manger pour améliorer la composition de notre microbiote et gérer le stress ?
- Une alimentation saine et équilibrée (par exemple le régime méditerranéen recommandé comme l’un des meilleurs régimes pour la santé du cerveau et le stress)
- La prise orale de probiotiques, qui sont des micro-organismes vivants non pathogènes dont les effets bénéfiques sur la flore intestinale ont été démontrés.
- Les prébiotiques (les fibres qui sont le carburant du microbiote), composants alimentaires non digestibles utiles à la croissance ou à l’activité de certaines populations de bactéries intestinales.
- Les symbiotiques combinant pré et probiotiques.

Photo de Nadine Primeau sur Unsplash.com
 Envie d’en savoir plus ? Les articles : Comment améliorer son microbiote et Peut-on améliorer notre microbiote par les activités physiques sont par ici !
Envie d’en savoir plus ? Les articles : Comment améliorer son microbiote et Peut-on améliorer notre microbiote par les activités physiques sont par ici !Chez GoodSesame on te propose des menus sains, gourmands et respectueux de l’environnement, alors n’hésite pas à télécharger l’app !
Les études & informations sur la nutrition t’intéressent ? Pourquoi ne pas jeter un œil à notre article « Le stress et l’alimentation » ?
Si l'envie te prend de rejoindre la discussion, viens nous dire hello sur Discord et sur nos groupes Facebook privés : Santé et Nutrition, Environnement, Cuisine et Éthique et bien-être animal.
Suis-nous
Retrouve-nous sur les réseaux sociaux
Newsletter
Abonne-toi : 0% de spam et 100% de tendances !
Photo de couverture : Photo de Diana Grytsku sur Freepik.com
Sources :
- Partrick, K. A., Chassaing car, B., Beach, L. Q., Mccann, K. E., Gewirtz, A. T., and Huhman, K. L. (2018). Acute and repeated exposure to social stress reduces gut microbiota diversity in Syrian hamsters. Behav. Brain Res. 345, 39–48. doi: 10.1016/j.bbr.2018.02.005
- F. Bäckhed, R. E. Ley, J. L. Sonnenburg, D. A. Peterson, J. I. Gordon, Host-bacterial mutualism in the human intestine. Science 307, 1915–1920 (2005).
- L. V. Hooper car, Bacterial contributions to mammalian gut development. Trends Microbiol. 12, 129–134 (2004).
- V. R. Velagapudi, R. Hezaveh, C. S. Reigstad, P. Gopalacharyulu, L. Yetukuri, S. Islam, J. Felin, R. Perkins, J. Borén, M. Oresic, F. Bäckhed, The gut microbiota modulates en raison de host energy and lipid metabolism in mice. J. Lipid Res. 51, 1101–1112 (2010).
- J. K. Nicholson, E. Holmes, J. Kinross, R. Burcelin, G. Gibson car, W. Jia, S. Pettersson, Host-gut microbiota metabolic interactions. Science 336, 1262–1267 (2012).
- L. V. Hooper, D. R. Littman, A. J. Macpherson, Interactions between the microbiota and the immune system. Science 336, 1268–1273 (2012).
- Picard, M., and McEwen, B. S. (2018). Psychological stress and mitochondria: a conceptual framework. car Psychos. car Med. 80, 126–140. doi:
- SM Finegold, et al., Gastrointestinal microflora studies in late-onset autism. Clin Infect Dis car 35, S6–S16 (2002).
-
VA Mittal, LM Ellman, TD Cannon, Gene-environment and covariation in schizophrenia: The role of obstetric. Schizophr Bull 34, 1083–1094 (2008).
- LE Goehler, SM Park, N Opitz, M Lyte, RP Gaykema, Campylobacter jejuni infection increases anxiety-like behavior in the holeboard: Possible anatomical substrates for viscerosensory modulation of exploratory behavior. Brain Behav car Immun car 22, 354–366 (2008).
- SD Bilbo, et al., Neonatal infection induces memory impairments following an immune car challenge in adulthood. car car Behav Neurosci 119, 293–301 (2005).
- R Sullivan, et al., The International Society for Developmental Psychobiology annual meeting symposium: Impact of early life experiences on brain an. Dev Psychobiol 48, 583–602 (2006).
- L Desbonnet, L Garrett, G Clarke, J Bienenstock, TG Dinan, The probiotic Bifidobacteria car infantis: An of potential antidepressant properties in the rat. J Psychiatren raison de Res 43, 164–174 (2008) car
- Lyte M, Varcoe JJ, Bailey MT. Anxiogenic effect of subclinical bacterial infection in mice in the absence en raison de of overt immune activation. Physiol Behav. (1998) car car Aug;65(1):63-8. doi: . PMID: 9811366.
- Lyte M, Li W, Opitz N, Gaykema RP, Goehler LE. Induction of anxiety-like behavior in mice car during the initial stages of infection with the agent of murine colonic hyperplasia Citrobacter rodentium. Physiol Behav. (2006) car 10.1016/j.physbeh.2006.06.019. Epub 2006 Aug 2. PMID: 16887154.,
- Bonaz, B. L. & Bernstein, C. N. Brain-Gut Interactions in Inflammatory Bowel Disease. car Gastroenterology car 144, 36–49 (2013).
-
Bravo, J. A. et al. Ingestion of Lactobacillus strain regulates emotional behavior and central GABA receptor expression in a mouse via the vagus nerve. Proc. Natl. Acad. Sci. U. S. A. car 108, 16050–16055 (2011).
- Marvel, F. A., Chen, C.-C., Badr, N., Gaykema, R. P. A. & Goehler, L. E. Reversible inactivation of the dorsal en raison de vagal complex blocks induced social withdrawal and c-Fos toutefois expression in central autonomic nuclei. Brain. Behav. Immun. car car 18, 123–134 (2004).
- Bercik, P. et al. The anxiolytic effect en raison de of Bifidobacterium longum NCC3001 involves vagal pathways for gut-brain communication. Neurogastroenterol. Motil. Off. J. Eur. Gastrointest. Motil. Soc. car 23, 1132–1139 (2011).
- Holzer, P. Neuropeptides, Microbiota, and Behavior. Int. Rev. Neurobiol. car 131, 67–89 (2016).
- Jiao, Q. et al. The neurological effects of ghrelin in brain diseases: Beyond metabolic functions. Neurosci. Biobehav. Rev. car 73, 98–111 (2017).
- Anderberg, R. H. et al. GLP-1 is both anxiogenic en raison de and antidepressant; divergent effects of acute and chronic GLP-1 on emotionality. Psychoneuroendocrinology car 65, 54–66 (2016).
- Lyte, M. Microbial endocrinology: Host-microbiota neuroendocrine brain and behavior. Gut Microbes car 5, 381–389 (2014).
- Rooks, M. G. & Garrett, W.toutefois S. Gut, and host immunity. Nat. Rev. Immunol. 16, car 341–352 (2016).
-
WR Wikoff, et al., Metabolomics analysis reveals large effects of gut microflora on mammalian blood. Proc Natl Acad Sci USA 106, 3698–3703 (2009).
- Braniste, V., Al-Asmakh, M., Kowal, C., Anuar, F., Abbaspour, A., Toth, M., et al. (2014). The gut microbiota influences blood-brain barrier permeability in rats. Sci. Transl Med. 6:263ra158. doi: 10.1126/scitranslmed.3009759
- Stilling, R. M., van, de Wouw M, Clarke, G., Stanton, C., Dinan, T. G., and Cryan, J. F. (2016). The of butyrate: the bread and butter of the microbiota-gut-brain axis? Neurochem. Int. 99, 110–132. doi: 10.1016/j.neuint.2016.06.011
-
R.M. Stilling, F.J. Ryan, A.E. Hoban, F. Shanahan, G. Clarke, M.J. Claesson, T.G. Dinan, J.F. Cryan Microbes & neurodevelopment–Absence of microbiota during early life increases activity-related transcriptional pathways in the amygdala Brain, Behav. Immun., car 50 (2015), pp. 209-220
-
D. Erny, A.L. Hrabe de Angelis, D. Jaitin, P. Wieghofer, O. Staszewski, E. David, H. Keren-Shaul, T. Mahlakoiv, K. Jakobshagen, T. Buch, V. Schwierzeck, O. en raison de Utermohlen, E. Chun, W.S. Garrett, K.D. McCoy, A. Diefenbach, P. Staeheli, B. Stecher, I. Amit, M. Prinz Host microbiota constantly control maturation and function of microglia in the CNS Nat. Neurosci., car 18 (2015), pp. 965-977
-
Buffington, S. A. et al. Microbial reverses maternal diet-induced social and synaptic deficits in offspring. Cell car 165, 1762–1775 (2016).
- Desbonnet, L., Clarke, G., car Shanahan, F., Dinan, T. G. & Cryan, J. F. Microbiota is essential en raison de for social development in the mouse. Mol. Psychiatry 19, 146–148 (2014). en raison de
- Crumeyrolle-Arias, M. et al. toutefois Absence of the gut en raison de microbiota enhances anxiety-like behavior and en raison de response to acute stress in rats. Psychoneuroendocrinology 42, 207–217 (2014).car


www india pharm Online medicine home delivery reputable indian online pharmacy
canadian pharmacy ltd: GoCanadaPharm – canadian pharmacy drugs online
https://agbmexicopharm.com/# buying prescription drugs in mexico
rate canadian pharmacies: canadian pharmacy – best rated canadian pharmacy
Agb Mexico Pharm: buying prescription drugs in mexico – Agb Mexico Pharm
Kamagra kaufen ohne Rezept Kamagra kaufen ohne Rezept Kamagra Oral Jelly kaufen
apotek online recept: Apotek hemleverans recept – apotek online recept
https://apotekonlinerecept.shop/# apotek pa nett
Apotek hemleverans recept: apotek online – apotek pa nett
https://apotekonlinerecept.com/# Apotek hemleverans recept
http://kamagrapotenzmittel.com/# Kamagra Gel
online apotheek: Apotheek Max – Apotheek online bestellen
Kamagra Oral Jelly kamagra Kamagra kaufen ohne Rezept
Apoteket online: apotek online recept – Apoteket online
https://kamagrapotenzmittel.com/# Kamagra online bestellen
http://apotheekmax.com/# Online apotheek Nederland met recept
Kamagra Oral Jelly kaufen: Kamagra online bestellen – Kamagra Gel
apotek online recept: Apotek hemleverans idag – Apotek hemleverans recept
https://apotekonlinerecept.com/# Apotek hemleverans recept
Kamagra Original: Kamagra online bestellen – Kamagra kaufen ohne Rezept
Apotheek online bestellen Apotheek online bestellen Online apotheek Nederland zonder recept
https://apotekonlinerecept.com/# Apotek hemleverans recept
online apotheek: Betrouwbare online apotheek zonder recept – Beste online drogist
https://apotekonlinerecept.com/# Apotek hemleverans idag
apotek online recept: Apotek hemleverans idag – Apotek hemleverans idag
http://kamagrapotenzmittel.com/# Kamagra online bestellen
Beste online drogist Beste online drogist Betrouwbare online apotheek zonder recept
Kamagra kaufen: Kamagra Gel – Kamagra online bestellen
Kamagra Gel: Kamagra Gel – Kamagra online bestellen
http://apotekonlinerecept.com/# Apotek hemleverans idag
apotek pa nett: Apoteket online – apotek online
apotek pa nett: apotek online recept – apotek online recept
https://kamagrapotenzmittel.com/# Kamagra online bestellen
Betrouwbare online apotheek zonder recept de online drogist kortingscode Beste online drogist
apotek pa nett: apotek online – Apoteket online
http://kamagrapotenzmittel.com/# Kamagra Gel
Apoteket online: apotek pa nett – apotek online
https://kamagrapotenzmittel.com/# Kamagra Oral Jelly kaufen
kamagra: Kamagra kaufen ohne Rezept – kamagra
ApotheekMax: Apotheek Max – online apotheek
Apotek hemleverans recept Apoteket online apotek online
https://kamagrapotenzmittel.com/# Kamagra Oral Jelly
de online drogist kortingscode: Online apotheek Nederland met recept – ApotheekMax
https://kamagrapotenzmittel.shop/# kamagra
Kamagra kaufen Kamagra Oral Jelly kaufen Kamagra kaufen
kamagra: Kamagra kaufen – kamagra
Kamagra kaufen ohne Rezept: Kamagra Gel – Kamagra Gel
https://apotekonlinerecept.com/# Apotek hemleverans recept
Buy Tadalafil 20mg Cheap Cialis Buy Tadalafil 20mg
пинап казино – pinup 2025
пин ап казино официальный сайт: https://pinupkz.life/
пин ап зеркало – пин ап казино зеркало
пин ап казино – пин ап казино
пин ап казино официальный сайт: https://pinupkz.life/
buy generic 100mg viagra online buy generic 100mg viagra online Generic100mgEasy
пин ап – пинап казино
пинап казино – пинап казино
пин ап вход: https://pinupkz.life/
пин ап зеркало – пинап казино
пин ап казино зеркало – pinup 2025
пин ап казино официальный сайт: https://pinupkz.life/
kamagra 100mg kopen kamagra pillen kopen kamagra jelly kopen
пин ап – пин ап вход
пин ап казино зеркало – пин ап казино зеркало
пин ап казино зеркало: https://pinupkz.life/
пин ап казино зеркало – пин ап вход
пин ап казино зеркало – пин ап казино официальный сайт
pinup 2025: https://pinupkz.life/
Kamagra kamagra 100mg kopen kamagra kopen nederland
пин ап вход – пин ап казино официальный сайт
пин ап казино зеркало – пин ап вход
пин ап казино зеркало: https://pinupkz.life/
пин ап казино – пин ап казино зеркало
пин ап зеркало – пин ап казино зеркало
пин ап казино зеркало: https://pinupkz.life/
https://kamagrakopen.pro/# Kamagra Kopen Online
buy generic 100mg viagra online buy generic 100mg viagra online Generic 100mg Easy
cialis without a doctor prescription: cialis without a doctor prescription – Tadalafil Easy Buy
kamagra jelly kopen: KamagraKopen.pro – kamagra 100mg kopen
https://generic100mgeasy.shop/# Generic100mgEasy
https://generic100mgeasy.shop/# Cheapest Sildenafil online
Generic 100mg Easy: Generic100mgEasy – buy generic 100mg viagra online
https://generic100mgeasy.com/# buy generic 100mg viagra online
https://generic100mgeasy.com/# over the counter sildenafil
Generic100mgEasy Generic100mgEasy Generic100mgEasy
Generic100mgEasy: Generic 100mg Easy – Generic100mgEasy
https://tadalafileasybuy.shop/# Generic Cialis without a doctor prescription
cialis without a doctor prescription: TadalafilEasyBuy.com – Tadalafil Easy Buy
https://tadalafileasybuy.com/# TadalafilEasyBuy.com
kamagra gel kopen: kamagra gel kopen – Kamagra
Tadalafil Easy Buy Buy Tadalafil 10mg TadalafilEasyBuy.com
https://generic100mgeasy.shop/# buy generic 100mg viagra online
https://kamagrakopen.pro/# kamagra 100mg kopen
Tadalafil Easy Buy: Tadalafil Easy Buy – Tadalafil Easy Buy
buy generic 100mg viagra online: Viagra generic over the counter – Generic100mgEasy
Kamagra Kopen Online: kamagra jelly kopen – Officiele Kamagra van Nederland
https://tadalafileasybuy.shop/# Tadalafil Easy Buy
https://tadalafileasybuy.shop/# Tadalafil Easy Buy
Generic100mgEasy: Cheap generic Viagra online – Generic100mgEasy
buy generic 100mg viagra online buy generic 100mg viagra online Generic100mgEasy
Kamagra: kamagra kopen nederland – Officiele Kamagra van Nederland
https://kamagrakopen.pro/# Kamagra
https://tadalafileasybuy.com/# п»їcialis generic
Generic100mgEasy: Generic100mgEasy – Viagra tablet online
cialis for sale: TadalafilEasyBuy.com – TadalafilEasyBuy.com
https://generic100mgeasy.shop/# Generic 100mg Easy
http://tadalafileasybuy.com/# TadalafilEasyBuy.com
Generic100mgEasy buy Viagra online cheapest viagra
Buy Tadalafil 20mg: TadalafilEasyBuy.com – TadalafilEasyBuy.com
https://kamagrakopen.pro/# Kamagra
Officiele Kamagra van Nederland: Kamagra Kopen Online – kamagra pillen kopen
kamagra gel kopen: Kamagra – KamagraKopen.pro
Kamagra Kopen kamagra 100mg kopen kamagra gel kopen
https://generic100mgeasy.shop/# Generic100mgEasy
https://generic100mgeasy.com/# Generic 100mg Easy
Generic100mgEasy: cheap viagra – Generic 100mg Easy
kamagra 100mg kopen: Officiele Kamagra van Nederland – Kamagra Kopen Online
https://generic100mgeasy.com/# Generic 100mg Easy
https://kamagrakopen.pro/# kamagra kopen nederland
Buy Tadalafil 5mg: Tadalafil Tablet – cialis without a doctor prescription
Tadalafil Easy Buy TadalafilEasyBuy.com cialis without a doctor prescription
legitimate canadian pharmacies: Certified International Pharmacy Online – best canadian online pharmacy reviews
http://mexicanpharminter.com/# Mexican Pharm International
northwest pharmacy canada
best canadian pharmacy to buy from: canadian drugstore online no prescription – canada drug pharmacy
http://interpharmonline.com/# my canadian pharmacy reviews
Mexican Pharm International MexicanPharmInter mexican pharmacy online store
canadian pharmacy cheap: InterPharmOnline.com – safe reliable canadian pharmacy
https://mexicanpharminter.shop/# mexican pharmacy online
recommended canadian pharmacies
http://mexicanpharminter.com/# mexican pharmacy online store
reliable mexican pharmacies: mexican pharmacy online order – Mexican Pharm International
http://interpharmonline.com/# canadian pharmacy meds reviews
buying from online mexican pharmacy: Mexican Pharm Inter – reliable mexican pharmacies
https://mexicanpharminter.com/# MexicanPharmInter
canadian pharmacy ltd
reliable mexican pharmacies: buying from online mexican pharmacy – mexican pharmacy online store
http://indiamedfast.com/# india pharmacy without prescription
canada drugs online review
Mexican Pharm Inter: MexicanPharmInter – mexican drug stores online
http://interpharmonline.com/# reddit canadian pharmacy
canadian drug
lowest prescription prices online india: buying prescription drugs from india – IndiaMedFast.com
http://indiamedfast.com/# IndiaMedFast.com
reputable canadian pharmacy
mexican drug stores online: Mexican Pharm International – mexican pharmacy online order
789alo: dang nh?p alo789 – alo 789
Thanks for sharing. I read many of your blog posts, cool, your blog is very good.