Les acides aminés sont des composés organiques qui s’assemblent pour former des protéines dans ton corps. Ils jouent un rôle important dans la vie humaine. Environ 20 % du poids du corps humain adulte est constitué d’acides aminés. En effet, pour une personne pesant 70 kg, 14 kg sont des acides aminés. Grâce à cet article, tu sauras absolument tout sur les acides aminés et leurs propriétés !
Sommaire
- Que sont les acides aminés et les acides aminés essentiels ?
- Les besoins en acides aminés essentiels
- Les acides aminés essentiels et leurs fonctions spécifiques
- Recettes savoureuses et riches en acides aminés essentiels
Que sont les acides aminés et les acides aminés essentiels ?
Il existe 20 acides aminés au total, et ils entrent chacun dans l’une de ces deux catégories :
- Essentiels (à ingérer dans l’organisme avec la nourriture)
- Non essentiels (ces types d’acides aminés peuvent être synthétisés par l’organisme)
Les acides aminés essentiels
Comme ton corps ne peut pas fabriquer lui-même les neuf acides aminés essentiels, tu dois les obtenir à partir des aliments que tu manges. Ils comprennent :
- L’histidine
- L’isoleucine
- La leucine
- La lysine
- La méthionine
- La phénylalanine
- La thréonine
- Le tryptophane
- La valine
Lorsque l’on examine attentivement les acides aminés, qui sont les éléments de base de l’organisme, le plus important n’est pas la quantité de protéines que nous consommons par jour, mais la quantité d’acides aminés essentiels que nous introduisons dans le corps (1), (2), (3)

Photo de master1305 sur Freepik.com
Fonctions générales
Matières premières des substances porteuses dans le sang
L’hémoglobine, l’albumine, la transferrine (sont trois protéines qui transportent des substances dans le sang) et les lipoprotéines (HDL, LDL, VLDL, connues sous le nom de cholestérol du sang) sont composées de ces acides aminés.
Création d’enzymes
Les acides aminés sont responsables de toutes les réactions chimiques de notre organisme; amylase, pepsine, lipase (ce sont trois enzymes de digestion) et ALT, AST (enzymes du métabolisme du foie).
Transformation des graisses en énergie
La L-carnitine est une substance chimique fabriquée dans le cerveau, le foie et les reins. Elle aide l’organisme à transformer les graisses en énergie. La L-carnitine est importante pour les fonctions cardiaques et cérébrales, les mouvements musculaires et de nombreux autres processus corporels. La L-Carnitine est un peptide bien connu et largement utilisé comme complément alimentaire. Elle est essentielle au métabolisme des lipides et se compose de deux acides aminés, la lysine et la méthionine.
Apport d’énergie aux muscles
La créatine est une substance que l’on trouve naturellement dans les cellules musculaires. Elle est utilisée pour la fourniture instantanée d’énergie aux muscles dans le corps. Elle se compose de deux acides aminés, la glycine et l’arginine.
Création d’hormones
La quasi-totalité des hormones (l’insuline, le glucagon, l’hormone de croissance, etc.) ont pour origine des acides aminés. Seules les hormones stéroïdiennes telles que la testostérone, les œstrogènes et la cortisone sont synthétisées par des enzymes à partir du cholestérol, et non à partir d’acides aminés. L’hormone thyroïdienne provient d’une acide aminé, la tyrosine (3), (4), (5).
Séquence génétique
Les gènes relient les acides aminés pour former des protéines. Toutes les protéines commencent par le codon AUG, un acide aminé appelé la méthionine. C’est le codon de démarrage de la séquence du génome humaine (4), (6).
Photo de julien Tromeur sur Unsplash.com
Comment expliquer les carences en acides aminés ?
Signes généraux de carence
La carence en protéines se produit rarement de manière isolée. Elle s’accompagne généralement d’une carence en énergie et en autres nutriments résultant d’un apport alimentaire insuffisant. Les symptômes sont le plus souvent observés chez les enfants des pays en développement. Lorsque l’apport en protéines est exceptionnellement faible, on observe des signes physiques – retard de croissance, mauvaise musculation, œdèmes, cheveux fins et fragiles, lésions cutanées – et des modifications biochimiques, notamment un faible taux d’albumine sérique et des déséquilibres hormonaux. Les œdèmes et la perte de masse musculaire et de cheveux sont les signes les plus importants chez les adultes. Une carence de cette gravité est très rare en Europe, sauf si elle est la conséquence de conditions pathologiques et d’une mauvaise prise en charge médicale des personnes souffrant de maladies graves (7).

Photo de kroshka__nastya sur Freepik.com
Une carence en acides aminés est possible et peut être due à de nombreuses causes. Les raisons sont les suivantes (1) :
- Vieillissement
- Stress chronique
- Dépression
- Prise de médicaments (antiacides, antibiotiques, médicaments de traitement chimique)
- Régimes hypoprotidiques (les régimes pauvres en protéines)
- Alimentation peu variée
- Consommation excessive de produits industriels
- Maladies du système digestif
- Malabsorptions
- Excrétion excessive urinaire
- Déséquilibre vitaminique et minéral
- Traumatismes, brûlures, chirurgies, maladies chroniques
- Chirurgie de l’obésité.
Les besoins en acides aminés essentiels
Les besoins en acides aminés sont pris en compte avec les besoins en protéines. De plus, il est primordial de varier les sources d’alimentation afin de combler la totalité des besoins.
Les apports nutritionnels conseillés (ANC) en protéines varient selon les personnes : enfants, adultes, femmes enceintes, personnes âgées : chacun a des besoins différents. Pour un homme sédentaire sain, le besoin estimé est de 0,6 à 0,8 gramme de protéines par kg de poids corporel (8, 9). Selon les données de l’enquête INCA1 (24), l’apport moyen en protéines est de 1,4 g/kg/j. Les besoins sont donc largement couverts dans les pays développés. Les protéines devraient se situer entre 11 et 15% de la ration journalière mais en réalité elles représentent 17% (10, 11).
Certains auteurs recommandent même 2 à 3 g/kg/j pour les athlètes de force, mais des apports plus élevés (à partir de 3,5 g/kg/j) ne représentent aucun bénéfice, le surplus se transforme en résidus gras lors du catabolisme protéique. Oui, tu as bien entendu ! L’excès de protéines est stocké sous forme de graisse !
Les protéines dans les aliments courants
Teneur en protéines de certains aliments (12, 13) :
| Aliment | Quantité de protéines pour 100g |
|---|---|
| Steak haché 5% de matière grasse | 25,5g |
| Saumon cuit à la vapeur | 20,8g |
| Cabillaud | 23,1g |
| Jambon | 20,3g |
| Escalope de dinde | 24,6g |
| Œuf cru | 12,7g |
| Tofu | 9,9g |
| Escalope végétale ou steak à base de soja | 15,5g |
| Lentilles vertes cuites | 10g |
| Amandes | 25g |
| Quinoa cru | 14g |
Voici un autre tableau montrant la séquence d’acides aminés des aliments. Le quinoa, bien que d’origine végétale, se distingue par sa parfaite séquence d’acides aminés…
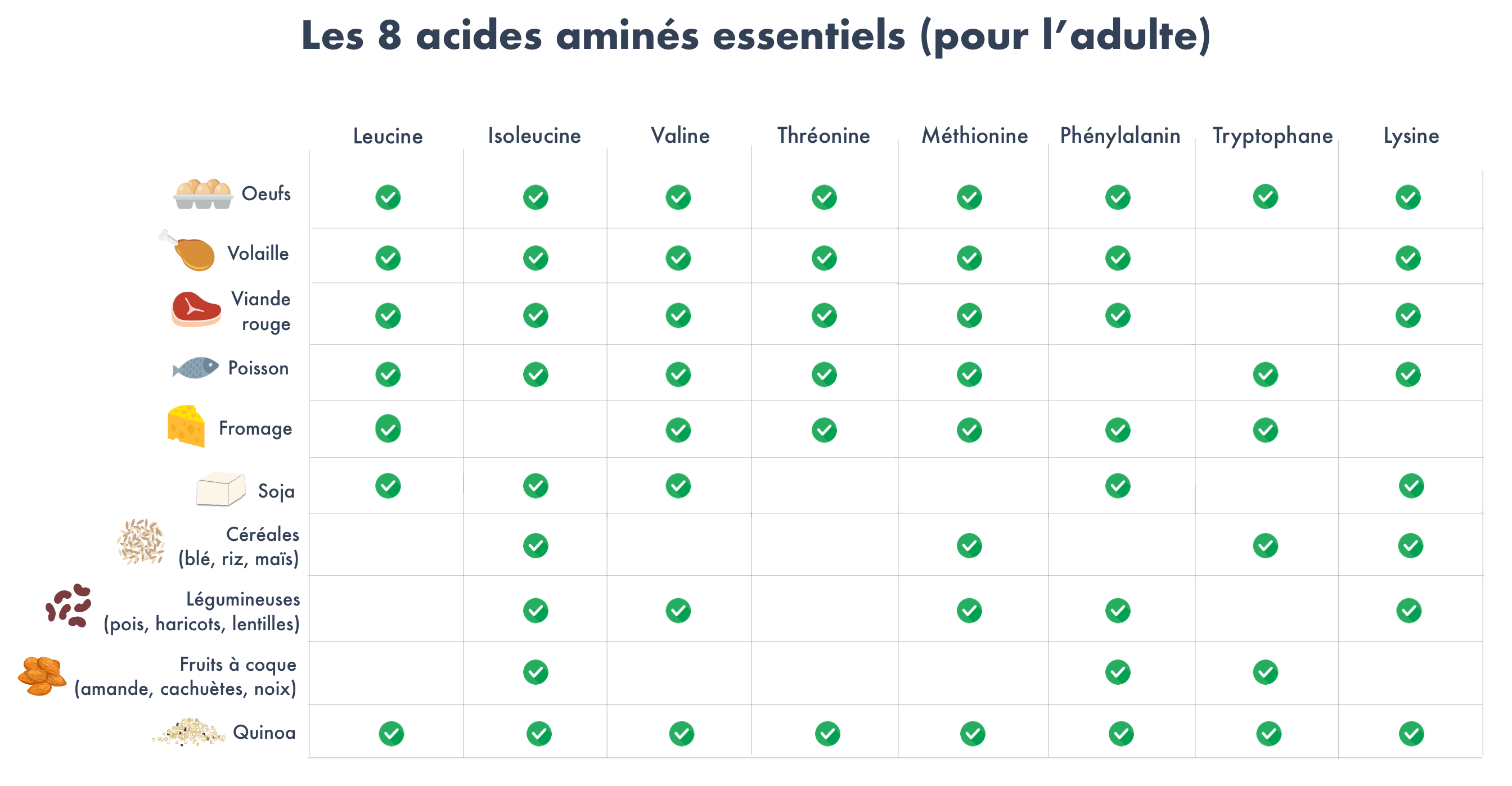
Acides aminés présents dans les aliments
Étant donné que presque aucune des protéines végétales ne fournit une séquence d’acides aminés complète, il est important de varier l’alimentation dans un régime à base de plantes.
Ceren, nutritionniste GoodSesame
Les acides aminés essentiels et leurs fonctions spécifiques
Avant d’examiner en détail chacun des acides aminés essentiels, jetons un coup d’œil à un résumé de toutes les caractéristiques générales ! En plus de servir d’éléments constitutifs des protéines, les AA jouent un rôle dans :
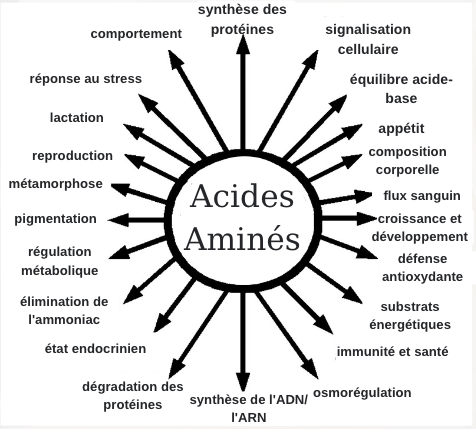
Rôles des Acides Aminés (AA) dans la nutrition et l’homéostasie (équilibre) du corps entier.
La méthionine
Le rôle essentiel de la méthionine est d’initier la synthèse des protéines (14),
Rôle d’antioxydant :
Les résidus de méthionine partagent au moins deux fonctions avec sa sœur soufrée (ces deux derniers transportent du soufre), la cystéine : défense antioxydante (14, 15) et régulation de la fonction cellulaire (16, 17, 18).
Les résidus de méthionine constituent un important mécanisme de défense antioxydant : une variété d’oxydants réagissent facilement avec la méthionine pour former du sulfoxyde de méthionine, et les résidus de méthionine exposés en surface créent une concentration extrêmement élevée de réactif, disponible comme piège à oxydants efficace. Cela signifie que la méthionine est oxydée afin que d’autres structures importantes de l’organisme ne soient pas oxydées et endommagées. Cela se produit de manière dynamique dans le corps (14-19).
Les acides aminés contenant du soufre neutralisent les radicaux libres (les oxydants). Le soufre est nécessaire à la synthèse du glutathion qui est un antioxydant l’un des plus puissants (20).
Fourniture de méthyle et muscles :
La créatine est la source d’énergie immédiate des muscles. On la synthétise à partir de la glycine, de l’arginine et grâce à un groupe méthyle provenant de la S-adénosylméthionine (SAM) qui est la forme active de la méthionine (21-23).
- Le soufre de la méthionine prend place dans la structure de la kératine. La kératine est essentielle pour la santé des cheveux, de la peau et des ongles (24).
- Les niveaux de carnitine jouent un rôle essentiel dans la production d’énergie. Ils sont corrélés à l’apport en acides aminés essentiels, méthionine et lysine (comme des substrats pour sa synthèse interne) (25, 26).

Photo de Tyler Nix sur Unsplash.com
Dépression :
Les résultats obtenus lors d’études préliminaires en double aveugle soutiennent l’hypothèse selon laquelle la forme active de méthionine peut avoir des effets antidépresseurs (27).
La lysine
Action anti inflammatoire :
Nous avons constaté que la Poli Lysine (PL) (un homopolymère de L-lysine relié par des liaisons peptiques) réduisait la sécrétion des agents inflammatoires. D’autre part, l’expression génétique de ces agents (qui s’appellent TNF-α, IL-6 et IL-1β) a été inhibée par la supplémentation en PL (C’est un effet bénéfique pour les maladies inflammatoires de l’intestin) (28).
Le virus de l’herpès simplex (HSV) : Des essais contrôlés randomisés en double aveugle ont montré que la supplémentation en lysine est efficace dans le traitement de HSV en raison de ses propriétés antivirales (29, 30).
Os & Muscles & Peau :
L’ostéoporose : La lysine favorise l’absorption du calcium et réduit l’excrétion urinaire du calcium. La supplémentation en lysine et en arginine réduit la perte osseuse et combat l’ostéoporose en augmentant la production de collagène (31).
La lysine a une fonction importante dans la constitution des liaisons entre les molécules pour construire les fibrilles et les fibres de collagène important pour la peau (32).

Photo de Joel Ambass sur Unsplash.com
Diminution de l’anxiété :
La lysine se comporte comme un antagoniste (l’opposition, l’inhibition) des récepteurs de la sérotonine, empêchant ainsi partiellement les réponses à l’anxiété (33). La carence en L-lysine est connue pour augmenter le risque d’anxiété chez les humains (34, 35).
Le tryptophane
Le tryptophane est un autre acide aminé essentiel.
Sommeil
Il est le précurseur de la sérotonine, connue sous le nom d’hormone du bonheur. Le tryptophane est transformé en sérotonine et la sérotonine en mélatonine (l’hormone du sommeil). Grâce ce dernier, la mélatonine régule le rythme biologique de l’organisme.
L’obscurité et le sommeil sont essentiels à la synthèse de la mélatonine. Le tryptophane est un activateur de la sérotonine et de l’hormone neurosécrétoire mélatonine pour le sommeil/éveil (36).
Stress-Anxiété – Dépression :
Une carence alimentaire en L-tryptophane, L-phénylalanine ou L-tyrosine entraîne une faible synthèse de sérotonine en raison du manque de disponibilité de ces éléments constitutifs et cette carence alimentaire est associée à l’anxiété (37-39).
On sait que la supplémentation alimentaire en L-tryptophane augmente la synthèse de la sérotonine chez les rats et les humains (37, 38, 40), ce qui confirme une approche nutritionnelle du traitement de l’anxiété. Le 5-hydroxytryptophane (5-HTP), (le précurseur du tryptophane), augmente les niveaux de sérotonine synthétisée chez les humains (41, 42). Le 5-HTP et le tryptophane augmentent les niveaux de sérotonine dans le cerveau et sont connus pour améliorer le sentiment de bien-être (43-45).
Enfin, l’augmentation de l’apport en tryptophane du cerveau favorise la synthèse et la libération de la sérotonine. Amélioration de l’anxiété et des troubles du comportement sont dus à une carence en sérotonine (46, 47).
L’insuline (l’hormone que nous sécrétons après avoir consommé notamment des glucides) provoque le passage dans le tissu musculaire des acides aminés leucine, isoleucine, valine, avec lesquels le Tryptophane est en compétition dans le sang lorsqu’il passe dans le tissu cérébral, et la concentration sanguine de Tryptophane augmente.
Pour cette raison, les glucides qui augmentent rapidement l’insuline et les sucreries et le chocolat à forte teneur en tryptophane provoquent le bonheur.

Photo de Jacqueline Munguia sur Unsplash.com
BCAA (Acides aminés à chaîne ramifiée)
Leucine, Isoleucine, Valine : Impliqués dans la synthèse des protéines, l’énergie et le métabolisme du stress. Les BCAA peuvent réguler le taux de synthèse et de dégradation des protéines dans les muscles et les autres organes.
Humeur
Ils agissent sur l’état psychologique. Les BCAA et les autres acides aminés (AA) se lient aux mêmes protéines porteuses pour être transportés vers le cerveau. Ils sont en compétition les uns avec les autres et leur ratio dans le cerveau. Cela peut influencer la synthèse de neurotransmetteurs spécifiques (les messagers), ce qui peut influencer le comportement d’un organisme (49, 50).
Fatigue
Les BCAA ont une action de régulation du glycogène (les réserves de glucose dans le corps) et ont une relation inverse avec les niveaux de tryptophane dans le cerveau qui est le précurseur de la sérotonine. La sérotonine est un médiateur de la fatigue centrale. Ainsi, une supplémentation en BCAA peut prévenir la fatigue lors d’un exercice intense, et un régime enrichi en BCAA peut améliorer le métabolisme des protéines musculaires, le maintien de l’organisme, ainsi que l’exercice aérobie (50, 51). En termes simples, pendant l’exercice, les BCAA passent dans le muscle et cessent d’entrer en compétition avec le tryptophane. Ainsi, chacun fait son travail !
Muscles
Ils augmentent la masse musculaire, la force musculaire et l’endurance. De plus, ils améliorent la récupération après l’exercice. Ils sont donc importants pour la croissance et la réparation des os et des muscles.
Source d’énergie
Les BCAA ont un meilleur rendement énergétique que le glucose. Par exemple, l’oxydation complète de la leucine dans le muscle produit plus d’énergie que l’utilisation complète du glucose sous forme d’énergie (52)
Synthèse des protéines
On observe également que les BCAA régulent le renouvellement des protéines dans les muscles en inhibant la dégradation des protéines et en favorisant leur synthèse (53-55).
Performance
On a également constaté que la supplémentation en protéines enrichies en BCAA est bénéfique chez les animaux et les humains en augmentant la performance à l’effort (52).

Photo de Jonathan Chng sur Unsplash.com
Immunité
Les trois BCAA sont absolument nécessaires à la croissance et à la prolifération des lymphocytes (nos agents de lutte contre les organismes pathogènes). Les BCAA sont également importants pour l’activité des lymphocytes T cytotoxiques et des cellules tueuses naturelles (encore, agents bénéfiques de notre système immunitaire) (56).
Une étude humaine (57) sur des patients ayant subi une intervention chirurgicale montre qu’une supplémentation accrue en BCAA entraîne une augmentation des lymphocytes sanguins postopératoires, des paramètres immunitaires plus élevés et une meilleure récupération. Bassit et al. (58) ont observé ses effets bénéfiques sur des triathlètes d’élite masculins concernant les paramètres immunitaires.
Diabète
Ils régulent le taux sanguin de sucre, leur ratio dans le sang augmente en cas de résistance à l’insuline et de diabète.
Il existe une forte corrélation entre les BCAA circulants et la prédiction du diabète (58). Dans une étude récente, il a été constaté que les patients atteints de diabète de type 2, qui présentaient une altération de la glycémie à jeun (taux de sucre sanguin), avaient également des niveaux élevés de BCAA par rapport aux individus sains (59, 52).
Enfin, une augmentation du taux sanguin de BCAA est associée à un risque élevé de trouble métabolique et de résistance à l’insuline future, ou de diabète de type 2 (60).
Que déclare l’EFSA sur les BCAA ?
 L’EFSA (Autorité européenne de sécurité des aliments) effectue des évaluations scientifiques afin de contribuer à garantir que les allégations nutritionnelles et de santé figurant sur l’étiquetage et la publicité des denrées alimentaires sont pertinentes et correctes, et peuvent ainsi aider les consommateurs à faire des choix alimentaires sains. Elle commence donc à autoriser certaines allégations de santé sur les nutriments. Il y a aussi certaines allégations de santé que l’EFSA permet (61), par exemple, sur les BCAA ! Examinons-les ensemble !
L’EFSA (Autorité européenne de sécurité des aliments) effectue des évaluations scientifiques afin de contribuer à garantir que les allégations nutritionnelles et de santé figurant sur l’étiquetage et la publicité des denrées alimentaires sont pertinentes et correctes, et peuvent ainsi aider les consommateurs à faire des choix alimentaires sains. Elle commence donc à autoriser certaines allégations de santé sur les nutriments. Il y a aussi certaines allégations de santé que l’EFSA permet (61), par exemple, sur les BCAA ! Examinons-les ensemble !
Croissance ou maintien de la masse musculaire
Les effets allégués sont : « réduction la dégradation des protéines après l’exercice », « augmentation la synthèse des protéines », « récupération/augmentation de la synthèse des protéines dans les muscles squelettiques pendant la récupération après un exercice de force prolongé » et « métabolisme musculaire ». La population cible est considérée comme étant la population générale.
Atténuation du déclin de la puissance musculaire
L’effet revendiqué est « atténue le déclin de la puissance produite après un exercice en haute altitude ».
La population cible est considérée comme étant des personnes actives effectuant un entraînement en haute altitude.
Récupération plus rapide de la fatigue musculaire après l’exercice
Les effets allégués sont « métabolisme musculaire » et « favorise la récupération musculaire après l’exercice ».
On considère que la population cible est constituée de personnes actives dans la population générale.
Amélioration de la fonction cognitive après l’exercice
L’effet allégué est « améliore la performance mentale après l’exercice ». Le Comité suppose que la population cible est constituée d’individus actifs dans la population générale. La fonction cognitive comprend la mémoire, l’attention (concentration), l’apprentissage, l’intelligence et la résolution de problèmes, qui sont des concepts bien définis et peuvent être mesurés par des tests cognitifs psychométriques validés.
Réduction de l’effort perçu pendant l’exercice
L’effet revendiqué est le suivant : « Les BCAA améliorent la performance pendant un exercice soutenu ». Le Comité considère que la population cible est constituée d’individus actifs dans la population générale.
La phénylalanine
Stress
Elle permet la synthèse de la dopamine (dans un premier temps) et l’adrénaline et la noradrénaline (dans un second temps). Ces trois neurotransmetteurs contribuent au bon fonctionnement du système nerveux et hormonal. Ils agissent par ce biais sur les troubles de l’humeur, l’amélioration de la concentration et de la vigilance et, ainsi, sur le bien-être général (62).
Fatigue
De plus, la phénylalanine en favorisant la sécrétion d’hormones telles que la dopamine et en stimulant le système nerveux central, présente un intérêt dans une stratégie « anti-fatigue ». En effet, la dopamine en agissant sur la motivation, la concentration et le mouvement, est un neurotransmetteur favorisant le tonus et la vitalité (63).
Peau
La phénylalanine est impliquée dans la synthèse de la mélanine. La mélanine est fabriquée par les cellules situées au plus profond de l’épiderme. Elle est retrouvée dans la peau, les cheveux et les yeux. Elle joue un rôle photo protecteur contre les rayonnements ultraviolets du soleil, qui accentuent le processus de vieillissement (64).

Photo de Autumn Goodman sur Unsplash.com
L’Histidine
Antioxydant
L’histidine a montré une activité antioxydante, empêchant la glycation et la lipoxydation (dommages des lipides) qui sont des marqueurs de stress oxydatif (dommages des cellules) (65).
Allergies & Immunité
Elle est utilisée pour soigner les états allergiques, car elle est un antagoniste de l’histamine (agent du système immunitaire et marqueur d’allergie) (66).
Performance musculaire
Une supplémentation pourrait améliorer la fatigue lors de l’effort sportif (67).
Inflammations digestives chroniques
Il a été démontré que les maladies inflammatoires de l’intestin, telles que la maladie de Crohn et la rectocolite hémorragique, pouvaient être influencées par positivement l’administration d’histidine (68).
Dermatite atopique (eczéma)
Une dermatite atopique (eczéma) et une diminution des taux d’histamine dans le plasma et l’urine sont fréquemment observés chez les sujets déficients en histamine (69).
Fatigue mentale
Un essai croisé en double aveugle, contrôlé par placebo, a permis une amélioration de la sensation de fatigue avec l’administration de l’histidine lors des tâches de mémoire de travail, chez des personnes souffrant de fatigue et de perturbation du sommeil (70).

Photo de Kinga Cichewicz sur Unsplash.com
La thréonine
Immunité :
La thréonine (L-Thr) stimule le système immunitaire en participant à la production des anticorps (71).
Des informations montrent que la thréonine peut avoir un effet actif sur les systèmes de défense antioxydants et qu’il est l’un des acides aminés qui transportent une petite fraction du cuivre dans le sang (72). Par conséquent, un niveau alimentaire approprié de L-Thr peut contribuer à la capacité antioxydante (73).
Digestion
La thréonine participe activement à la digestion au niveau de l’absorption des nutriments dans le sang.
Par rapport aux autres acides aminés essentiels, la teneur en L-Thr dans les protéines de l’intestin représente jusqu’à 30% ce qui révèle que la thréonine peut contribuer à la fonctionnalité et au maintien de l’intestin (74).
Utile en cas de troubles intestinaux et d’indigestion, la thréonine a également été utilisée pour soulager l’anxiété et la dépression légère (75, 72).
Recettes
Voici 3 idées recettes savoureuses et riches en acides aminés essentiels !
Chez GoodSesame on te propose des menus sains, gourmands et respectueux de l’environnement, alors n’hésite pas à télécharger l’app !
Les études & informations sur la nutrition t’intéressent ? Pourquoi ne pas jeter un œil à notre article « L’alimentation pour la fatigue et le sommeil » ?
Si l'envie te prend de rejoindre la discussion, viens nous dire hello sur Discord et sur nos groupes Facebook privés : Santé et Nutrition, Environnement, Cuisine et Éthique et bien-être animal.
Suis-nous
Retrouve-nous sur les réseaux sociaux
Newsletter
Abonne-toi : 0% de spam et 100% de tendances !
Crédit photo de couverture : Master1305 provenant de Freepik.com
Sources :
- Aydın Duygu, Dr. Acides Aminés, 2e édition, (2017), Istanbul Tıp kitabevleri. Aydin, Dr Acide aminé essentiels,
- Janaway, R. C., Percival, S. L., & Wilson, A. S. (2009). Decomposition of Human Remains. In S. L. Percival (Éd.), Microbiology and Aging : Clinical Manifestations (p. 313‑334). Humana Press. https://doi.org/10.1007/978-1-59745-327-1_14
- Textbook of medical physiology / Arthur C. Guyton, John E. Hall.-11th ed. ISBN 0-7216-0240-1
- Lieberman M. Marks’ Basic Medical Biochemistry Fourth, North American Edition Edition Lippincott Williams & Wilkins 2013
- Richard S. Ed. Lord Laboratory Evaluations for Integrative and Functional Medicine 2nd Edition Metametrix Institute, 2008
- https://jdidcott999.wordpress.com/cell-division-genes-prontiens/
- Allowances, N. R. C. (US) S. on the T. E. of the R. D. (1989). Protein and Amino Acids. In Recommended Dietary Allowances : 10th Edition. National Academies Press (US). https://www.ncbi.nlm.nih.gov/books/NBK234922/
- AFSSA. Apport en protéines : consommation, qualité, besoins et recommandations. 2007 p. 461.
- ANSES. Actualisation des repères du PNNS : élaboration des références nutritionnelles. 2016 p. 329.
-
AFSSA. Etude Individuelle Nationale des Consommations Alimentaires 2 (INCA2 ). 2009.
- ANSES. Etude individuelle nationale des consommations alimentaires 3 (INCA 3). 2017 p. 566.
- Bouget, C. (s. d.). Protéines et acides aminés : Utilisations par les sportifs et conseils à l’officine. 152
- Ciqual Table de composition nutritionnelle des aliments [Internet]. Disponible sur: https://ciqual.anses.fr/
- Levine, R., Moskovitz, J., & Stadtman, E. (2001). Oxidation of Methionine in Proteins : Roles in Antioxidant Defense and Cellular Regulation. IUBMB Life, 50(4), 301‑307. https://doi.org/10.1080/713803735
- Levine, R. L., Mosoni, L., Berlett, B. S., and Stadtman, E. R. (1996) Methionine residues as endogenous antioxidants in proteins. Proc. Natl. Acad. Sci. USA 93, 15036–15040. 2. Gonias, S. L., Swaim, M. W.,
- Massey, M. F., and Pizzo, S. V. (1988) cisdichlorodiammineplatinum (II) as a selective modi er of the oxidationsensitive reactive-center methionine in alpha 1-antitrypsin. J. Biol. Chem. 263, 393–397.
- Brot, N., and Weissbach, H. (1991) Biochemistry of methionine sulfoxide residues in proteins. BioFactors 3, 91–96.
- Vogt, W. (1995) Oxidation of methionine residuesin proteins: Tools, targets, and reversal. Free Radic. Biol. Med. 18, 93–105.
- Luo, S., & Levine, R. L. (2009). Methionine in proteins defends against oxidative stress. The FASEB Journal, 23(2), 464‑472. https://doi.org/10.1096/fj.08-118414
-
Reed, D. J., & Orrenius, S. (1977). The role of methionine in glutathione biosynthesis by isolated hepatocytes. Biochemical and Biophysical Research Communications, 77(4), 1257‑1264. https://doi.org/10.1016/S0006-291X(77)80115-0
- da Silva, R. P., Nissim, I., Brosnan, M. E., & Brosnan, J. T. (2009). Creatine synthesis : Hepatic metabolism of guanidinoacetate and creatine in the rat in vitro and in vivo. American Journal of Physiology-Endocrinology and Metabolism, 296(2), E256‑E261. https://doi.org/10.1152/ajpendo.90547.2008
- Du Vigneaud, V., Cohn, M., Chandler, J. P., Schenck, J. R., & Simmonds, S. (1941). The utilization of the methyl group of methionine in the biological synthesis of choline and creatine. Journal of Biological Chemistry, 140, 625‑641.
- Brosnan, J. T., Brosnan, M. E., Bertolo, R. F. P., & Janet A. Brunton. (2007). Methionine : A metabolically unique amino acid. Livestock Science, 112(1), 2‑7. https://doi.org/10.1016/j.livsci.2007.07.005
- Haneke, E., & Baran, R. (2011). Micronutrients for Hair and Nails. In J. Krutmann & P. Humbert (Éds.), Nutrition for Healthy Skin : Strategies for Clinical and Cosmetic Practice (p. 149‑163). Springer. https://doi.org/10.1007/978-3-642-12264-4_14
- Krajcovicová-Kudlácková, M., Simoncic, R., Béderová, A., Babinská, K., & Béder, I. (2000). Correlation of carnitine levels to methionine and lysine intake. Physiological Research, 49(3), 399‑402.
- Tanphaichitr, V., & Leelahagul, P. (1993). Carnitine metabolism and human carnitine deficiency. Nutrition (Burbank, Los Angeles County, Calif.), 9(3), 246‑254.
- Papakostas, G. I., Alpert, J. E., & Fava, M. (2003). S-adenosyl-methionine in depression : A comprehensive review of the literature. Current Psychiatry Reports, 5(6), 460‑466. https://doi.org/10.1007/s11920-003-0085-2
- Mine, Y., & Zhang, H. (2015). Anti-inflammatory Effects of Poly-l-lysine in Intestinal Mucosal System Mediated by Calcium-Sensing Receptor Activation. Journal of Agricultural and Food Chemistry, 63(48), 10437‑10447. https://doi.org/10.1021/acs.jafc.5b03812
- Griffith RS. Success of L-lysine therapy in frequently recurrent Herpes simplex infection. Treatment and prophylaxis. Dermatologica. 1987;175:183-190.
-
Milan N. Lysine prophylaxis in recurrent Herpes simplex labialis: a double-blind, controlled crossover study. Acta Derm Venereol. 1980;60:85-87.
- Civitelli R. Dietary L-lysine and calcium metabolism in humans. Nutrition 1992;8:400-405.
- Frey J, Raby N. Lysine et collagène [Lysine and collagen]. Ann Biol Clin (Paris). 1991;49(1):36-9. French. PMID: 1904695.
- Smriga M, Torii K. L-Lysine acts like a partial serotonin receptor 4 antagonist and inhibits serotonin-mediated intestinal pathologies and anxiety in rats. Proc Natl Acad Sci U S A. 2003 Dec 23;100(26):15370-5. doi: 10.1073/pnas.2436556100. Epub 2003 Dec 15. PMID: 14676321; PMCID: PMC307574.
- Ghosh S, Smriga M, Vuvor F, et al. Effect of lysine supplementation on health and morbidity in subjects belonging to poor peri-urban households in Accra, Ghana. Am J Clin Nutr. 2010;92(4):928–39.
- Smriga M, Ghosh S, Mouneimne Y, et al. Lysine fortification reduces anxiety and lessens stress in family members in economically weak communities in Northwest Syria. Proc Natl Acad Sci USA. 2004;101(22):8285–88.
- Jones BE. Neurobiology of waking and sleeping. Handb Clin Neurol. 2011;98:131–49
- Hood SD, Hince DA, Davies SJ, et al. Effects of acute tryptophan depletion in serotonin reuptake inhibitor-remitted patients with generalized anxiety disorder. Psychopharmacology (Berl) 2010;208(2):223–32.
- Toker L, Amar S, Bersudsky Y, et al. The biology of tryptophan depletion and mood disorders. Isr J Psychiatry Relat Sci. 2010;47(1):46–55.
- Roiser JP, Levy J, Fromm SJ, et al. The effect of acute tryptophan depletion on the neural correlates of emotional processing in healthy volunteers. Neuropsychopharmacology. 2008;33(8):1992–2006.
-
Feurté S, Gerozissis K, Regnault A, Paul FM. Plasma Trp/LNAA ratio increases during chronic ingestion of an alpha-lactalbumin diet in rats. Nutr Neurosci. 2001;4(5):413–18.
- Trachte GJ, Uncini T, Hinz M. Both stimulatory and inhibitory effects of dietary 5-hydroxytryptophan and tyrosine are found on urinary excretion of serotonin and dopamine in a large human population.acides aminés essentiels Neuropsychiatr Dis Treat. 2009;5:227–35.
- . Croonenberghs J, Verkerk R, Scharpe S, et al. Serotonergic disturbances in autistic disorder: L-5-hydroxytryptophan administration to autistic youngsters increases the blood concentrations of serotonin in patients but not in controls. Life Sci. 2005;76(19):2171–83.
- Young SN, Leyton M. The role of serotonin in human mood and social interaction. Insight from altered tryptophan levels. Pharmacol Biochem Behav. 2002;71(4):857–65.
- Lakhan SE, Vieira KF. Nutritional therapies for mental disorders. Nutr J. 2008;7:2.
- Markus CR. Dietary amino acids and brain serotonin function; implications for stress-related affective changes. Neuromolecular Med. 2008;10(4):247-58.
- Lindseth G. The effects of dietary tryptophan on affective disorders. Arch Psychiatr Nurs. 2015Apr;29(2):102-7
- Schneider-Helmert D. Evaluation of L-tryptophan for treatment of insomnia: a review. Psychopharmacology (Berl). 1986;89:1-7
- Mawson, A. R., & Jacobs, K. W. (1978). Corn consumption, tryptophan, and cross-national homicide rates. Journal of Orthomolecular Psychiatry. https://scholar.google.com/scholar_lookup?title=Corn+consumption%2C+tryptophan%2C+and+cross-national+homicide+rates&author=Mawson%2C+A.R.&publication_year=1978
- B. Skeie, V. Kvetan, K. M. Gil, M. M. Rothkopf, E. A. Newsholme, and J. Askanazi, “Branch-chain amino acids: their metabolism and clinical utility,” Critical Care Medicine, vol. 18, no. 5, pp. 549–571, 1990.
-
J. D. Fernstrom, “Branched-chain amino acids and brain function,” Journal of Nutrition, vol. 135, supplement 6, pp. 1539S– 1546S, 2005.
- H. Kainulainen, J. J. Hulmi, and U. M. Kujala, “Potential role of branched-chain amino acid catabolism in regulating fat oxidation,” Exercise and Sport Sciences Reviews, vol. 41, no. 48, pp. 194–200, 2013.
- Monirujjaman, Md., & Ferdouse, A. (2014). Metabolic and Physiological Roles of Branched-Chain Amino Acids. Advances in Molecular Biology, 2014, 1‑6. https://doi.org/10.1155/2014/364976
- H. R. Freund and M. Hanani, “The metabolic role of branchedchain amino acids,” Nutrition, vol. 18, no. 3, pp. 287–288, 2002.
- A. L. Goldberg and R. Odessey, “Oxidation of amino acids by diaphragms from fed and fasted rats.,” The American Journal of Physiology, vol. 223, no. 6, pp. 1384–1391, 1972.
- M. G. Buse and S. S. Reid, “Leucine: a possible regulator of protein turnover in muscle,” Journal of Clinical Investigation, vol. 56, no. 5, pp. 1250–1261, 1975.
- P. C. Calder, “Branched-chain amino acids and immunity,” The Journal of Nutrition, vol. 136, supplement 1, no. 1, pp. 288S–293S, 2006.
- F. B. Cerra, J. E. Mazuski, E. Chute et al., “Branched chain metabolic support. A prospective randomized, double-blind trial in surgical stress,” acides aminés essentielsAnnals of Surgery, vol. 199, no. 3, pp. 286– 291, 1984. R. A. Bassit, L. A. Sawada, R. F. P. Bacurau et al., “Branchedchain amino acid supplementation and the immune response of long-distance athletes,” Nutrition, vol. 18, no. 5, pp. 376–379, 2002.
- B. C. Batch, K. Hyland, and L. P. Svetkey, “Branch chain amino acids: biomarkers of health and disease,” Current Opinion in Clinical Nutrition and Metabolic Care, vol. 17, no. 1, pp. 86–89, 2014.
- F. Xu, S. Tavintharan, C. F. Sum, K. Woon, S. C. Lim, and C. N. Ong, “Metabolic signature shift in type 2 diabetes mellitus revealed by mass spectrometry-based metabolomics,” Journal of Clinical Endocrinology and Metabolism, vol. 98, no. 6, pp. E1060–E1065, 2013.
-
Yoon, M.-S. (2016). The Emerging Role of Branched-Chain Amino Acids in Insulin Resistance and Metabolism. Nutrients, 8(7), 405. https://doi.org/10.3390/nu8070405
- EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA). (2010). Scientific Opinion on the substantiation of health claims related to branched-chain amino acids (BCAA) and growth or maintenance of muscle mass (ID 442, 444, 445, 447, 448, 451, 1478), attenuation of the decline in muscle power following exercise at high altitude (ID 443), faster recovery from muscle fatigue after exercise (ID 447, 448, 684,1478), improvement of cognitive function after exercise (ID 446), reduction in perceived exertion during exercise (ID 450) and “healthy immune system” (ID 449) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. EFSA Journal, 8(10), 1790. https://doi.org/10.2903/j.efsa.2010.1790
- Beckmann, H., M.A. Strauss, and E. Ludolph, Dl-phenylalanine in depressed patients: an open study. J Neural Transm, 1977. 41(2-3): p. 123-34.
- Cordeiro, L.M.S., et al., Physical exercise-induced fatigue: the role of serotonergic and dopaminergic systems. Braz J Med Biol Res, 2017. 50(12): p. e6432.
- Slominski, A., M.A. Zmijewski, and J. Pawelek, L-tyrosine and L-dihydroxyphenylalanine as hormone-like regulators of melanocyte functions. Pigment Cell Melanoma Res, 2012. 25(1): p. 14-27.
- Scavenging of singlet molecular oxygen by imidazole compounds: high and sustained activities of carboxy terminal histidine dipeptides and exceptional activity of imidazole-4-acetic acid 1990
- The therapeutic use of the amino acid histidine in allergy and shock—acides aminés essentiels “Histidine as a factor in histamine epinephrine balance” 1944
- Determinants of muscle carnosine content 2012
- (Smoothie 4) Dietary histidine ameliorates murine colitis by inhibition of proinflammatory cytokine production from macrophages 2009
-
Evidence that histidine is an essential amino acid in normal and chronically uremic man 1975
- The effect of histidine on mental fatigue and cognitive performance in subjects with high fatigue and sleep disruption scores 2015
- Saadatmand N., Toghyani M., Gheisari A. Effects of dietary fiber and threonine on performance, intestinal morphology and immune responses in broiler chickens. Anim. Nutr. 2019;5:248–255.
- Aydın Duygu, Dr. Acides Aminés, 2e édition, (2017), Istanbul Tıp kitabevleri. Aydin, Dr Acide aminé,
- Li, J. M., Zhang, X. Y., Yuan, C., Miao, L. P., Yan, H. X., Dong, X. Y., Lu, J. J., & Zou, X. T. (2016). Effects of dietary L-threonine levels on antioxidant capacity, digestive enzyme activities, and antibody production of Xinyang green-shell laying hens. Journal of Applied Poultry Research, 25(3), 422‑427. https://doi.org/10.3382/japr/pfw028
- M.R. Neutra, J.F. Forstner Gastrointestinal mucus: Synthesis, secretion and function L.R. Johnson (Ed.), Physiology of the Gastrointestinal Tract (2nd ed.), Raven Press, New York (1987), pp. 975-1009
- PubChem. (s. d.). L-Threonine. Consulté 28 juin 2022, à l’adresse https://pubchem.ncbi.nlm.nih.gov/compound/6288


de online drogist kortingscode: Apotheek Max – Apotheek online bestellen
https://kamagrapotenzmittel.com/# Kamagra kaufen
apotek pa nett: Apoteket online – apotek online
https://kamagrapotenzmittel.shop/# kamagra
Kamagra Original: Kamagra Original – Kamagra Oral Jelly
https://kamagrapotenzmittel.com/# Kamagra kaufen ohne Rezept
online apotheek Apotheek online bestellen Beste online drogist
Apotek hemleverans recept: apotek online recept – Apotek hemleverans recept
https://apotheekmax.com/# Apotheek online bestellen
apotek online recept: apotek online recept – apotek online
http://kamagrapotenzmittel.com/# Kamagra Original
http://kamagrapotenzmittel.com/# Kamagra Oral Jelly
Online apotheek Nederland met recept: Online apotheek Nederland met recept – online apotheek
online apotheek Betrouwbare online apotheek zonder recept Beste online drogist
apotek pa nett: Apoteket online – Apotek hemleverans recept
https://apotekonlinerecept.com/# Apoteket online
https://apotheekmax.com/# online apotheek
Apotek hemleverans recept: Apoteket online – apotek online
https://apotheekmax.com/# online apotheek
apotek pa nett: apotek online – apotek online recept
Kamagra kaufen ohne Rezept: Kamagra online bestellen – Kamagra Original
http://kamagrapotenzmittel.com/# Kamagra Gel
online apotheek Online apotheek Nederland zonder recept Apotheek Max
https://apotekonlinerecept.shop/# apotek online
Online apotheek Nederland met recept: Betrouwbare online apotheek zonder recept – Online apotheek Nederland zonder recept
Apotheek online bestellen: Apotheek Max – Beste online drogist
https://kamagrapotenzmittel.shop/# Kamagra Original
https://apotheekmax.com/# Apotheek online bestellen
Kamagra Oral Jelly: Kamagra Oral Jelly kaufen – Kamagra Gel
http://kamagrapotenzmittel.com/# Kamagra Original
Kamagra Gel Kamagra online bestellen Kamagra Gel
Online apotheek Nederland met recept: Online apotheek Nederland met recept – online apotheek
http://apotheekmax.com/# ApotheekMax
http://kamagrapotenzmittel.com/# Kamagra kaufen ohne Rezept
de online drogist kortingscode: Betrouwbare online apotheek zonder recept – Apotheek online bestellen
Kamagra Gel: Kamagra kaufen ohne Rezept – Kamagra Oral Jelly
https://kamagrapotenzmittel.com/# kamagra
apotek pa nett apotek online Apoteket online
http://apotheekmax.com/# Online apotheek Nederland met recept
Kamagra Oral Jelly: Kamagra Original – Kamagra Original
Betrouwbare online apotheek zonder recept: Beste online drogist – Apotheek online bestellen
https://apotheekmax.shop/# Online apotheek Nederland zonder recept
http://apotekonlinerecept.com/# Apotek hemleverans idag
Apotheek online bestellen: Betrouwbare online apotheek zonder recept – Online apotheek Nederland met recept
Online apotheek Nederland zonder recept: Online apotheek Nederland met recept – Online apotheek Nederland met recept
kamagra Kamagra Gel Kamagra Original
Les paris sportifs, ça peut vraiment être excitant, mais il faut savoir où on met les pieds. J’ai vite compris qu’il ne suffit pas de choisir un site au hasard. Sur https://betwinner-de-cote-divoire.com/ j’ai trouvé des infos claires sur l’inscription et les bonus, ce qui m’a bien aidé. Ce qui est essentiel, c’est de choisir une plateforme fiable, avec des paiements rapides et un bon service client. Et surtout, il faut garder la tête froide, ne jamais parier sur un coup de tête et surtout bien gérer son budget. C’est une question de stratégie, pas de chance.
пин ап казино зеркало – пин ап казино зеркало
пин ап зеркало – пин ап
пин ап: https://pinupkz.life/
TadalafilEasyBuy.com Tadalafil Easy Buy cialis without a doctor prescription
пин ап казино официальный сайт – pinup 2025
пин ап – пин ап зеркало
пин ап казино официальный сайт: https://pinupkz.life/
пин ап казино – пинап казино
пинап казино – пин ап казино официальный сайт
пинап казино: https://pinupkz.life/
kamagra 100mg kopen Kamagra Kopen Online Kamagra Kopen
pinup 2025 – пин ап казино
pinup 2025 – пин ап зеркало
pinup 2025: https://pinupkz.life/
пин ап – пин ап
пин ап вход – пинап казино
cheap viagra viagra without prescription Viagra tablet online
pinup 2025: https://pinupkz.life/
пинап казино – пин ап казино зеркало
пин ап вход – пин ап казино
пин ап казино официальный сайт: https://pinupkz.life/
pinup 2025 – пин ап казино зеркало
pinup 2025 – пин ап
пин ап вход: https://pinupkz.life/
cialis without a doctor prescription Tadalafil Easy Buy Generic Cialis without a doctor prescription
pinup 2025 – pinup 2025
пин ап казино зеркало – pinup 2025
kamagra jelly kopen: Kamagra Kopen – Kamagra
Kamagra Kopen Online: Kamagra Kopen – Kamagra Kopen
https://tadalafileasybuy.shop/# Cialis 20mg price
https://kamagrakopen.pro/# Kamagra Kopen
Generic100mgEasy: Cheap generic Viagra online – buy generic 100mg viagra online
Generic100mgEasy buy generic 100mg viagra online buy generic 100mg viagra online
Officiele Kamagra van Nederland: KamagraKopen.pro – kamagra pillen kopen
https://generic100mgeasy.shop/# Order Viagra 50 mg online
http://generic100mgeasy.com/# buy generic 100mg viagra online
Kamagra: kamagra kopen nederland – kamagra 100mg kopen
https://kamagrakopen.pro/# KamagraKopen.pro
https://generic100mgeasy.shop/# viagra canada
cialis without a doctor prescription: Generic Cialis without a doctor prescription – TadalafilEasyBuy.com
Kamagra Kopen kamagra kopen nederland kamagra 100mg kopen
http://generic100mgeasy.com/# Cheap generic Viagra online
https://generic100mgeasy.com/# buy generic 100mg viagra online
Kamagra Kopen: kamagra pillen kopen – kamagra kopen nederland
Generic100mgEasy: Generic100mgEasy – buy generic 100mg viagra online
kamagra jelly kopen: kamagra gel kopen – kamagra jelly kopen
http://generic100mgeasy.com/# Cheapest Sildenafil online
https://generic100mgeasy.shop/# generic sildenafil
kamagra kopen nederland: kamagra pillen kopen – kamagra kopen nederland
Buy generic 100mg Viagra online Generic 100mg Easy Viagra generic over the counter
buy generic 100mg viagra online: Generic 100mg Easy – Generic Viagra online
https://kamagrakopen.pro/# Kamagra Kopen
https://generic100mgeasy.shop/# Buy Viagra online cheap
buy generic 100mg viagra online: buy generic 100mg viagra online – buy generic 100mg viagra online
Kamagra Kopen Online: kamagra 100mg kopen – Kamagra
https://tadalafileasybuy.com/# Buy Tadalafil 5mg
https://tadalafileasybuy.com/# cialis without a doctor prescription
Tadalafil Easy Buy Tadalafil Easy Buy Tadalafil Easy Buy
KamagraKopen.pro: Kamagra Kopen Online – kamagra jelly kopen
Officiele Kamagra van Nederland: kamagra 100mg kopen – Officiele Kamagra van Nederland
http://generic100mgeasy.com/# Cheap Sildenafil 100mg
https://tadalafileasybuy.shop/# Tadalafil Easy Buy
Tadalafil Easy Buy: cialis without a doctor prescription – Buy Tadalafil 20mg
Generic 100mg Easy: Generic100mgEasy – buy generic 100mg viagra online
Tadalafil Tablet Buy Tadalafil 20mg TadalafilEasyBuy.com
https://kamagrakopen.pro/# kamagra jelly kopen
http://tadalafileasybuy.com/# TadalafilEasyBuy.com
kamagra pillen kopen: kamagra kopen nederland – kamagra kopen nederland
Officiele Kamagra van Nederland: Kamagra Kopen – KamagraKopen.pro
https://generic100mgeasy.shop/# Generic 100mg Easy
https://generic100mgeasy.com/# sildenafil over the counter
over the counter sildenafil buy generic 100mg viagra online Viagra Tablet price
Tadalafil Easy Buy: Tadalafil Easy Buy – Tadalafil Easy Buy
Officiele Kamagra van Nederland: Kamagra – kamagra pillen kopen
https://kamagrakopen.pro/# kamagra 100mg kopen
https://generic100mgeasy.shop/# buy generic 100mg viagra online
canadian pharmacy in canada: InterPharmOnline – canadian pharmacy tampa
http://indiamedfast.com/# IndiaMedFast.com
https://mexicanpharminter.shop/# Mexican Pharm International
canadapharmacyonline legit
canada rx pharmacy Online pharmacy USA canadian pharmacies online
canadian pharmacies that deliver to the us: Cheapest online pharmacy – canadian neighbor pharmacy
https://indiamedfast.com/# IndiaMedFast.com
canada pharmacy reviews
http://mexicanpharminter.com/# Mexican Pharm Inter
India Med Fast: order medicines online india – india online pharmacy store
global pharmacy canada: certified canada pharmacy online – my canadian pharmacy
https://indiamedfast.com/# IndiaMedFast.com
canadian online pharmacy reviews
https://indiamedfast.shop/# india pharmacy without prescription
online canadian pharmacy review certified canada pharmacy online canadian pharmacy sarasota
cheapest online pharmacy india: online pharmacy india – online pharmacy india
http://mexicanpharminter.com/# Mexican Pharm Inter
reputable canadian pharmacy
http://mexicanpharminter.com/# mexican pharmacy online
cheapest online pharmacy india: online medicine shopping in india – IndiaMedFast.com
canadian pharmacy review: most trusted canadian pharmacies online – canada rx pharmacy
legit canadian pharmacy canada pharmacy no prescription canadian pharmacy no scripts
https://indiamedfast.com/# online medicine shopping in india
canadian pharmacy meds reviews
https://indiamedfast.shop/# India Med Fast
buying prescription drugs from india: IndiaMedFast.com – cheapest online pharmacy india
buying prescription drugs from india: online medicine shopping in india – India Med Fast
http://interpharmonline.com/# canadian pharmacy meds
real canadian pharmacy
https://interpharmonline.shop/# canada rx pharmacy world
real canadian pharmacy most trusted canadian pharmacies online canadian neighbor pharmacy
IndiaMedFast.com: online medicine shopping in india – IndiaMedFast
https://indiamedfast.com/# online medicine shopping in india
canada cloud pharmacy
https://interpharmonline.com/# canada drugs online
Mexican Pharm International mexican pharmacy online store mexican drug stores online
canadianpharmacyworld com: highest rated canadian online pharmacy – best canadian online pharmacy reviews
alo 789 dang nh?p: alo789 dang nh?p – alo 789 dang nh?p
katana